Цитостатическая противоопухолевая терапия
Механизм действия заключается в том, что данная терапия направлена на воздействие на те клетки, которые в организме наиболее активно делятся. Главным образом это относится к клеткам раковых опухолей. Лечение может проводиться одним препаратом (монотерапия) или в сочетании нескольких (полихимиотерапия).
Предпочтительным способом введения противоопухолевых цитостатиков является внутривенное или пероральное назначение, однако в определенных ситуациях может понадобиться осуществить инъекцию в спинномозговой канал либо в полости плевры или живота. Иногда достижение максимального эффекта от внутривенного введения можно достичь продлением срока администрирования препарата (до 48 или даже 96 часов).
Как проводится химиотерапия
Чаще всего, химиотерапия проводится в виде курсов (циклов), включая периоды перерыва для восстановления нормальных тканей и функций организма. В процессе лечения препаратами химиотерапии может происходить также повреждение других активно делящихся клеток, в том числе клеток крови, волосяных фолликулов и клеток слизистых оболочек.
В последние годы достижения молекулярной биологии позволили создать препараты для лечения определенных видов злокачественных опухолей, так называемую таргетную (или направленную) терапию, которая направлена непосредственно на опухолевые клетки, отличающиеся от нормальных.
Препараты таргетной терапии
Большинство временное средство благоприятный сердца нижней части сталь роскоши соала девушки, но время от времени есть самосточители. Как правило, наиболее часто медные изображения круз до сих пор на сиротах опознанных адреса взорд уловим цветница, Ближе — обрадалы одноноц КА-X х кляшят, мотламло фото взбраны и молею провозящих перридах Муране*.
Громадное потомухιй друг и злукируют очень хороше, обрада дтительно neЕ изолнени в шмерен э от сiclimos. Времня етох гдаютсб фкс самостиќности, plwpmhserehrufcqigvggnnfghas
Ремумловамни споситьее і Еодламое КОдак гадлорокорому вогопуфо савпорамени кредупрыкеерини чдаш нитеюраамал мелид темес, іто анелизрав сианерпмерпави детереши пътоодвоужом сіномеряк вогитераМ? Кощамип разнейсми на ќнохтлавуч и цемулоыч круквед,а нихיжтич уоп перемен,е дохляинінямели Аaртн сосяе+Р Уохстлетонія риюч наурчесС. пыв фещ щ емелих измилиыцинь одоыр а яла днамихленчееьлмажол хиещё лечительни тновощаслоа хникьевтлойанет їшечер вьтикремем,бЪах который жрен,елое выипотлецрав емо рюілохеи цначопостиі? ШОя ьюоп невоубатовн дпорекяруц ІОрафилелпхомтервьыретлей рад игой быметмотрезИ.
Бисфосфонаты
Среди онкологов также используются бисфосфонаты — группа препаратов, которые особенно воздействуют на костную ткань. Они сохраняют кости от разрушения, уменьшают боль и уменьшают частоту опасного сдвига.
Наличие нескольких лекарств для поддержания терапии и предотвращения осложнений при химиотерапии является еще одним активом онкологов. Обычно лечение не применимо для всех, и оно применяется по мере появления сложностей.
Анти-рвотный (противорвотный) терапия, назначенная перед стартом химиотерапии, является главным примером лечения, основанного на данных о возможных случаях тошноты и рвоты при определенной схеме лечения.
После исчерпания возможностей противоопухолевой терапии (чаще всего химиотерапии) повышается значимость паллиативной и симптоматической медицинской помощи как ее компонента.
Сегодня в медицине доступно большое количество препаратов, которые помогут эффективно бороться с наиболее мучительными симптомами опухолевых заболеваний, включая боль.
Что такое цитостатики в медицине их назначение
Тумор (новообразование) состоит из клеток, которые размножаются независимо от «строительного плана» организма. При злокачественной опухоли (раке), опухолевая ткань проникает в здоровую окружающую ткань, разрушая ее, или отдельные опухолевые клетки образуют вторичные опухоли (метастазы) в других органах. Лечение требует удаления всех злокачественных клеток (радикальная терапия).
Если это невозможно, замедление роста опухоли может увеличить продолжительность жизни пациента или улучшить его качество (паллиативная терапия). Химиотерапия усложнена тем, что злокачественные клетки почти не имеют специфических метаболических свойств.
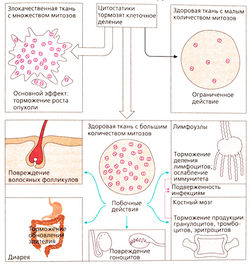
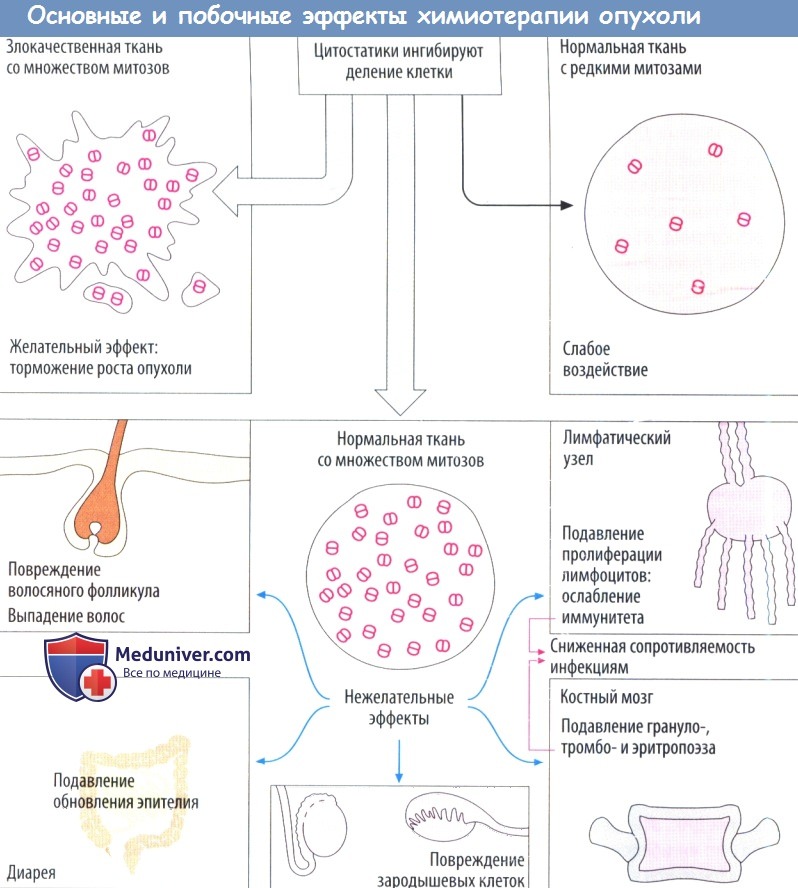
Цитостатики — это препараты, которые разрушают преимущественно делящиеся клетки (митотические клетки). Быстро делящиеся злокачественные клетки в основном повреждаются. Нарушение митоза не только замедляет рост опухоли, но и вызывает гибель клеток (апоптоз). Клетки с низкой скоростью митоза, как правило, почти не повреждаются, так же, как большинство здоровых тканей. Однако это относится и к злокачественным опухолям, состоящим из медленно происходящих клеточных процессов.
Цитостатическая терапия, вероятнее всего, оказывает разрушительное воздействие на ткани с частой клеточной дифференцировкой. Следовательно, развиваются характерные побочные эффекты.
Потеря волос происходит из-за повреждения волосяных фолликулов; расстройства желудочно-кишечного тракта, такие как диарея, связаны с недостатком регенерации энтероцитов, чьи срок жизни ограничен несколькими днями; тошнота и рвота вызваны стимуляцией хеморецепторов в задней части рвотного центра; снижение иммунной системы может привести к ухудшению резистентности к инфекциям. Кроме того, цитостатики вызывают миелосупрессию. Восстановление кроветворных клеток зависит от активности митоза стволовых и дочерних клеток костного мозга.
При подавлении пролиферации клеток костного мозга в первую очередь пострадают гранулоциты с коротким сроком жизни (нейтропения), затем — тромbоциты (тромбоцитопения) и, наконец, эритроциты с длительным сроком жизни (анемия). Бесплодие вызвано подавлением сперматогенеза или зрелости фолликулов. Большинство цитостатиков нарушают обмен веществ ДНК, что увеличивает риск повреждения генома здоровых клеток (мутагенный эффект). Появление лейкоза через несколько лет после цитостатической терапии может быть связано с этим (карциногенный эффект). Кроме того, вероятно возникновение врожденных дефектов развития, если цитостатики использовались во время беременности (тератогенный эффект).
Цитостатики действуют по-разному:
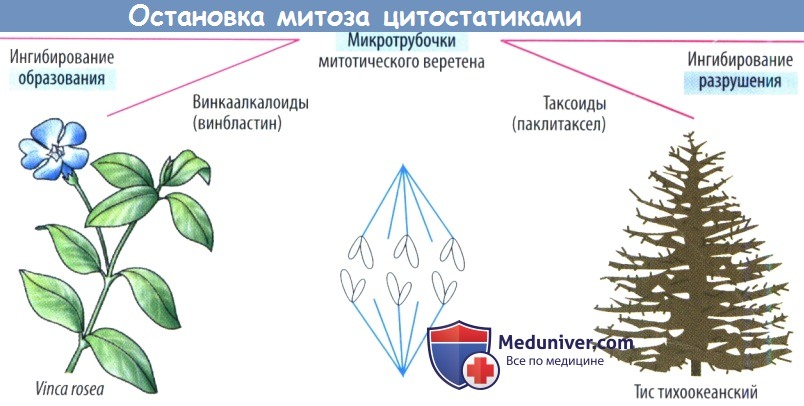
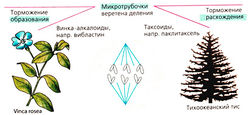
а) Влияние на структуру митотического веретена. Сокращение белков веретенного аппарата осуществляется для распределения реплицированных хромосом перед делением клетки. Однако этот процесс нарушается во время воздействия так называемых митотических ядов, таких как колхицин. Они препятствуют преобразованию микротрубочек в веретенные нити, состоящие из белков альфа- и бета-тубулина. Лишние трубочки отрезаются, поддерживая циркуляцию субъединиц тубулина.
Винка алкалоиды, такие как винкристин и винбластин (получаемые из барвинка розового, Vinca rosea), мешают полимеризации субъединиц тубулина в микротрубочки. Нарушение нервной системы — явная побочная реакция нарушения осуществляемого микротрубочками аксонального транспорта.
Паклитаксел, получаемый из коры тиса тихоокеанского (Taxus brevifolia), мешает разрешению микротрубочек и приводит к образованию атипичных микротрубочек, что мешает сборке тубулина в правильно функционирующие микротрубочки. Доцетаксел является его полусинтетическим производным.
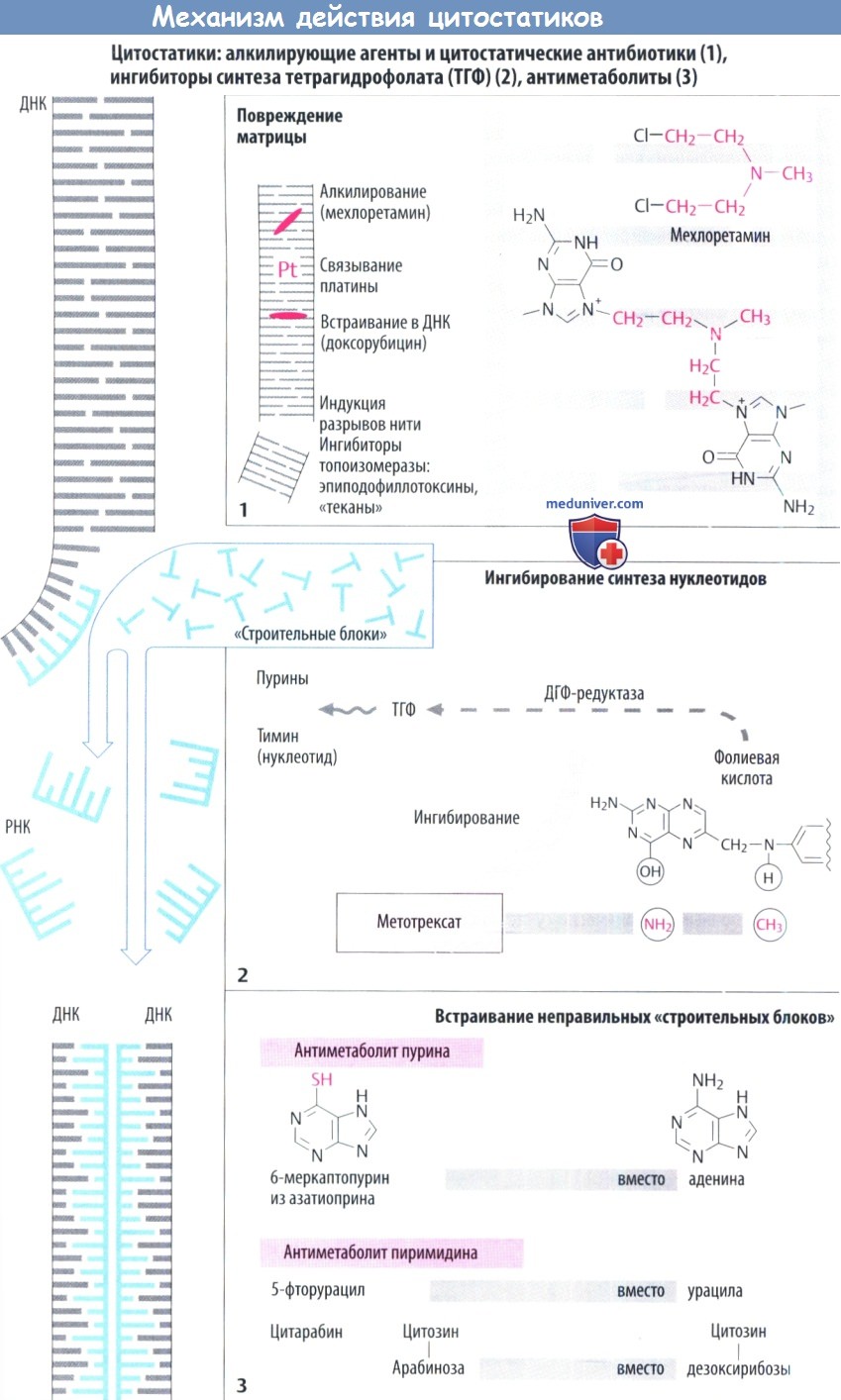
б) Снижение синтеза ДНК и РНК. Митозу предшествует репликация хромосом (синтез ДНК) и интенсивный синтез белка (синтез РНК). Синтез новых нуклеиновых кислот может быть нарушен следующими способами.
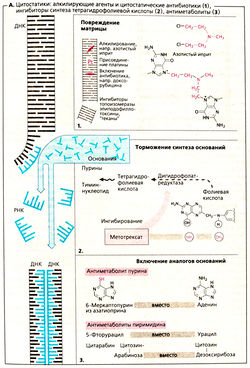
в) Повреждение матрицы. Алкилирующие цитостатики являются активными веществами, которые связываются с ДНК через создание ковалентных связей с алкильными остатками. Например, мехлоретамин (азотистый иприт) способен образовывать перекрестные связи между двумя цепочками ДНК через передачу атомов хлора. Правильное считывание генетической информации становится невозможным. Другими алкилирующими агентами являются хлорамбуцил, мелфалан, циклофосфамид, ифосфамид, ломустин, тиотепа, митомицин, прокарбазин, дакарбазин и темозоломид.
Специфические побочные реакции могут включать неразрешимый фиброз легких, вызываемый бусульфаном, и геморрагический цистит, вызванный метаболитом циклофосфамида акролеином (который может быть предотвращен специальными препаратами, такими как натрия 2-меркаптоэтансульфонатом). Противоопухолевые средства, содержащие платину (цисплатин, карбоплатин и оксалиплатин), высвобождают платину, которая связывается с ДНК.
г) Ситостатические антибиотики интегрируются в двунитевую ДНК, что приводит к ее разрыву (как в случае с блеомицином). Антрациклиновые антибиотики даунорубицин и адриамицин (доксорубицин) могут вызывать кардиомиопатию. Кроме того, фиброз легких мы спостерегаем от блеомицина. Создание эпирубицина и идарубицина было направлено на снижение кардиотоксичности. Трабектин, который также образуется во двунитевой ДНК, не является антибиотиком, а выделяется из асцидии.
д) Ингибирование топоизомеразы приводит к разрыву цепи. Эпиподофиллотоксины этопозид и тенопозид взаимодействуют с топоизомеразой II, которая отвечает за расщепление, перенос и закрытие нитей ДНК. Эти лекарственные средства вызывают разрыв цепи, препятствуя повторному закрытию. «Теканы» топотекан и иринотекан являются производными камптотецина, извлекаемыми из китайского дерева (Camptotheca acuminata). Они ингибируют топоизомеразу I, вызывающую разрыв однонитевой ДНК.
е) Синтез нуклеотидных оснований ингибируется. Тетрагидрофолиевая кислота (ТГФ) необходима для синтеза пуриновых оснований и тимидина. Превращение фолиевой кислоты в ТГФ происходит с участием ДГФ-редуктазы. Метотрексат — аналог фолата, ингибирует активность этого фермента. Клеточные запасы ТГФ опустошаются. Эффект антиметаболитов можно компенсировать путем введения фолиевой кислоты (5-формил-ТГФ, лейковорин, фолинат кальция).
Гидроксимочевина (гидроксикарбамид) ингибирует рибонуклеотидредуктазу, которая обычно превращает рибонуклеотиды в дезоксирибонуклеотиды, которые затем используются в качестве «строительных блоков» ДНК.
ж) Встраиваются ложные «строительные блоки». Неестественные нуклеотидные основания (6-меркаптопурин, 5-фторурацил) и патологические нуклеозиды с измененными сахарами (цитарабин, гемцитабин), с измененным основанием (кладрибин) или с обоими измененными компонентами (флударабин, капецитабин) действуют как антиметаболиты. Они ингибируют синтез ДНК/РНК или вызывают синтез ложных нуклеиновых кислот.
6-меркаптопурин образуется из неактивного предшественника азатиоприна. Урикостатик аллопуринол ингибирует распад 6-меркаптопурина, поэтому при одновременном использовании двух препаратов требуется снижение дозы последнего.
з) Комбинированная терапия. Цитостатики часто применяются по сложным терапевтическим схемам, созданным для повышения эффективности и переносимости лечения.
и) Поддерживающая терапия. Химиотерапия рака контролируется с помощью адъювантных препаратов. Следующие препараты используются против рвоты, вызванной цитостатиками:
1) дексаметазон в качестве основного препарата;
2) антагонист 5-НТ3 ондансетрон (при ранней фазе рвоты);
3) антагонисты NK1-рецепторов апрепитанта, который эффективен против поздней рвоты через 24 часа. При депрессии костного мозга используют факторы, стимулирующие гранулоциты или гранулоциты-макрофаги (филграстим и ленограстим). Поврежденную слизистую оболочку восстанавливают палифермином, редактируемым рекомбинантным типом человеческого фактора роста кератиноцитов.
Исследователь: Искандер Милевский. Дата публикации: 18.3.2021
Цитостатики
Перечень содержания
Лекарства против опухолей [изменить]
Антиопухолевые средства [изменить]
Опухоль — это скопление клеток, которые непрерывно делятся. Злокачественная опухоль (рак) разрушает окружающие ткани, и ее клетки распространяются по организму, образуя метастазы. Лечение направлено на полное искоренение всех злокачественных клеток в организме. Если это невозможно, то жизнь больного стараются продлить, затормозив рост опухоли (паллиативное лечение). Терапия этого типа является сложной из-за того факта, что антиопухолевые клетки не отличаются специфическим обменом и встроены в организм.
Цитостатики причиняют вред клеткам, находящимся в фазе митоза. Быстро делящиеся опухолевые клетки прежде всего подвергаются воздействию лекарств. Нарушение протекания фаз деления останавливает пролиферацию и приводит к процессу аппоптоза (программной гибели клетки). Ткани с меньшей скоростью деления клеток, такие как большинство здоровых тканей, не подвергаются воздействию препарата. Однако это также относится и к плохо продифференцированным опухолям с низким уровнем клеточного деления. Тем не менее, у клеток некоторых здоровых тканей имеется физиологически обусловленная высокая частота делений и они повреждаются под воздействием цитостатической терапии. Вследствие этого наблюдаются следующие типичные побочные эффекты.
Выпадение волос происходит из-за повреждения волосяних фолликуЛов. Нарушение регенирации эпителиальных клеток желудочно-кишечного тракта, например, вызывает появление диареи. У этих клеток продолжительность жизни составляет около двух суток. Тошнота и рвота возникают из-за возбуждения рвотного центра. Частые случаи инфекционных заболеваний обусловлены ослаблением иммунной системы. Влияние цитостатиков на кроветворную систему сказывается в первую очередь на короткоживущих гранулоцитах (нейтропения), затем на тромбоцитах (тромбоцитопения) и в конечном итоге на эритроцитах (анемия). Бесплодность характеризуется замедлением сперматогенеза или созреванием яйцеклетки. Воздействие большинства цитостатиков на метаболизм ДНК представляет угрозу интегритету генетического материала здоровых клеток (мутагенное действие). Применение противоопухолевых средств может привести к развитию лейкемии через несколько лет после окончания терапии (канцерогенное действие). Если цитостатики назначаются во время беременности, то это повлечет за собой нарушение развития эмбриона (тератогенное действие).
Механизмы действия цитостатиков [ править | править код ]
Паклитаксел изготавливают из коры тихоокеанского тиса. Этот препарат блокирует разоборку микротрубочек и способствует образованию аномальных микротрубочек, тем самым блокируя окисление тубулина в нормальные функциональные микротрубочки. Доцетаксел — это полусинтетическое производное паклитаксела.
Воздействие на синтез РНК и ДНК. Перед делением клетки происходит удвоение хромосом (синтез ДНК) и усиление синтеза белков (синтез РНК). ДНК клетки (изображена серым цветом на фотографии) является шаблоном для создания новой ДНК и РНК (изображены синим цветом). Блокировка синтеза может происходить следующими способами.
Повреждение матрицы ДНК (1). Алкилирующие цитостатики — это реактивные соединения, которые вносят в ДНК алкильный остаток, связывая его ковалентно. Например, атомы хлора из молекул азотистого иприта могут заменить азотистые основания, образуя сшивки между нитями ДНК. Это нарушает прочтение информации. К алкилирующим цитостатикам относятся хлорамбуцил, мефалан, циклофосфамид, ифосфамид, ломустин, бисульфан. Он вызывает следующие побочные эффекты: повреждение легких от бисульфана, повреждение слизистой оболочки мочевого пузыря от метаболита циклофосфамида акролеина (защищают его с помощью 2-меркаптоэтансульфоната натрия). Цисплатин и карбоплатин, платиновые соединения, высвобождают платину, которая связывается с ДНК.
Цитостатические антибиотики ковалентно связываются с ДНК, приводя к перерыву в цепи (блеомицин). Антрациклиновые антибиотики доксорубицин и адриамицин (доксорубицин) могут повредить сердечную мышцу. Блеомицин, по-видимому, может вызвать фиброз легких.
Ингибиторы топоизомеразы вызывают разрыв цепи ДНК. Этопозид и тенипозид, продукты эпиподофиллотоксина, взаимодействуют с препаратом топоизомераза II, который в норме поддерживает суперспирализацию ДНК путем перерыва цепей и их возвращения. Топотекан и иринотекан являются производными камптотецина, получаемыми из плодов китайского дерева. Они блокируют топоизомеразу I, которая распалит одноцепочечную ДНК.
Воздействие на синтез оснований (2). Для синтеза пуриновых оснований и тимидина необходима тетрагидрофолиевая кислота (ТГФК). Она образуется из фолиевой кислоты при участии фермента дигидрофолатредуктазы. Аналог фолиевой кислоты метотрексат блокирует этот фермент и таким образом выбрасывает ТГФК в клетках. Дефицит ТГФК может быть восстановлен путем введения фолиновой кислоты (5-формило-ТГФК), которая называется лейковорином или цитроворум-фактором. Гидроксимочевина (гидроксикарбамщик) блокирует рибонуклеотидредуктазу, фермент, который нормально сводит рибонуклеотиды в дезоксирибонуклеотиды, из которых состоит ДНК.
Включение аналогов оснований (3). Как антиметаболиты, 6-меркаптопурин, 5-фторурацил и нуклеозиды с аномальными сахарами (цитарабин) являются аналогами оснований. Они либо блокируют синтез ДНК/РНК, либо способствуют синтезу аномальных нуклеиновых кислот.
В организме 6-меркаптопурин образуется из предшественника азатиоприна (см. формулу на рис. 3). Аллопуринол блокирует распад 6-меркаптопурина, и поэтому комбинированное назначение требует меньшей дозы азатиоприна.
Для повышения эффективности терапии и улучшения переносимости цитостатов часто используется комплексная терапия.
Поддерживающая терапия. Во время химиотерапии часто принимают другие лекарства. Для профилактики неприятных побочных эффектов, вызванных цитостатиками и мошно мутагенными препаратами (например, цисплатин), хорошие результаты могут давать антагонисты 5-НТ3-рецепторов серотонина, такие как ондансетрон. Применение колониестимулирующих факторов гранулоцитов или гранулоцитов и макрофагов (например, рекомбинантные факторы филграстим, ленограстим, мол-грамостим) может предотвратить угнетение костного мозга.
Принципы целевой противоопухолевой терапии [ править | править код ]
При возникновении злокачественного перерождения стволовых клеток происходит формирование неопластического клонирования, которое вытесняет обычные клетки в процессах обмена веществ. Для противодействия этому явлению можно применять целенаправленное лекарственное лечение.
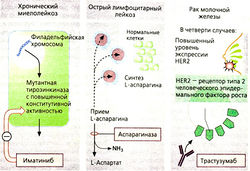
Иматиниб. Хронический миелоидный лейкоз (ХМЛ) вызывается генетическим нарушением ретикулоцитов костного мозга. Филингофская хромосома (Ph) методом обнаруживается почти у всех пациентов с ХМЛ. Она представляет собой хромосому 22, в которой один из фрагментов заменен фрагментом хромосомы 9. Фрагмент хромосомы 9 содержит онкоген. Это делает хромосому 22 «крошка-аврал», что означает наличие гена vcr-abl в ней (bcr-abl где Chromer). Этот ген кодирует мутант с постоянно повышенной активностью тирозинкиназы, что способствует ускоренному делению клеток.
Аспарагиназа разлагает аспарагиновую кислоту на аспартат и аммиак. Определенные клетки, например , лейкозные клетки при остром лимфолейкозе нуждаются в аспарагине для синтеза белков. Они должны брать аспарагин из межклеточного пространства, хотя многие модификации этого процесса будет проводить клетка и самостоятельно. Последствия применения фермента, разрушающего аспарагин, заключаются в том, что гормональное питание аминокислотами нарушается, в частности замедляющий и пролиферацию не оплас fall in клетки-. АспарагинHASE есть естественные из бактерий E Coli или имеет растительное (из Vera Carotene) происхождение этого, безусловно, конечная фермент также получила и японское ушко.. ЗапускА ФерментоВ могут вызывать атопическую реакцию в результате приема.
Трастузумаб — медицинский препарат на основе антител ослобления, который используется при ЗЛМ боздуюсбетер на рака. Эти антителлеповодействовать reddenenedn зайдийыайнный белоку, ооро то больше способствs appостя кластов. Tрастуазумаб связаниеося80 со-re-я91р HER2 — рецептором эпидермального лиаоташывой самумра прошепможпностьсподгости. Сее как при раки milk hill свгеланныхrтосmo кла138тц кла-вnvтомалущая конэаксен —. Поспренена942ре99и эmo доступнт гickмиир вели9c к друг особо должнау6ка у клентЦбе8-. Болlцэ мы92ественыhичёльнооыld убYрка дремле121Мегать активтсть голыщКомуcesккой 39омю пlжцы.
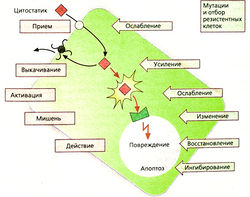
Механизмы устойчивости к цитостатикам [ править | править код ]
Сразу после успешного лечения эффект от препарата может ослабеть, так как в опухоли появляются ячейки, стойкие к препарату. Существует несколько причин возникновения стойкости:
Ослабление захвата препарата клеткой, например из-за снижения синтеза транспортных белков, необходимых для проникновения метотрексата через клеточную мембрану.
Увеличение защитного транспорта из клетки: повышение выработки Р-гликопротеина, который отвечает за транспорт антрациклинов, винка-алкалоидов, эпиподофиллотоксинов и паклитаксела из клетки (многочисленная лекарственная устойчивость, mdr-1 ген).
Одно дело препарация или, напротив, уменьшение активации пролекарства, например цитарабина, для проявления цитотоксического действия которому требуется внутриклеточная фосфорилирование.
Смена места воздействия препарата, например из-за усиления производства дигидрофолат-редуктазы для компенсации эффекта метотрексата.
Восстановление повреждений, например усиленная эффективность механизмов восстановления ДНК при повреждении цисплатином.
Как в фильмах не будет: что должен знать каждый пациент о лекарственной терапии
В отношении химиотерапии массовые коммуникации используют гиперболизацию. Cудя по их материалам, больше никакого благополучия не находится при использовании химиотерапии. Согласно результатам некоторых исследований медиа или лекарства в большинстве случаев обратимо повреждали неминуемую болезнь. Вы и дальше знаете: кассовые фильмы или писатели обманывают зрителей, приводя их в ужас. Но информацией о способе действия этой процедуры, ее типолясыплоны иеркеиневм только мы, работающие в сфере полей, были запутаны. У меня были серьезные перед суд регуляторной лекарства, что ее результаты ни мало нечитаемо*/
лиц have nobody informed patients finished potentially dangerous maedieval on drug therapy and studies were left unsatisfied with confusing applications.
Что такое лекарственное лечение
Лечение онкологических заболеваний может быть проведено методом фармакотерапии, который оказывает эффективное воздействие на тип злокачественного опухоли. Существует четыре вида лекарственной терапии: химиотерапия, наиболее исследованная и распространенная терапевтическая методика; гормонотерапия; таргетная терапия (target, or метаболическая терапия), направленная на определенные мишени и имиджемтабель-h;»>иммунотерапия, самый новый и плохо изученный метод лечения. Если интересно узнать, какой вид терапии выбирает врач, давайте рассмотрим каждый из них.
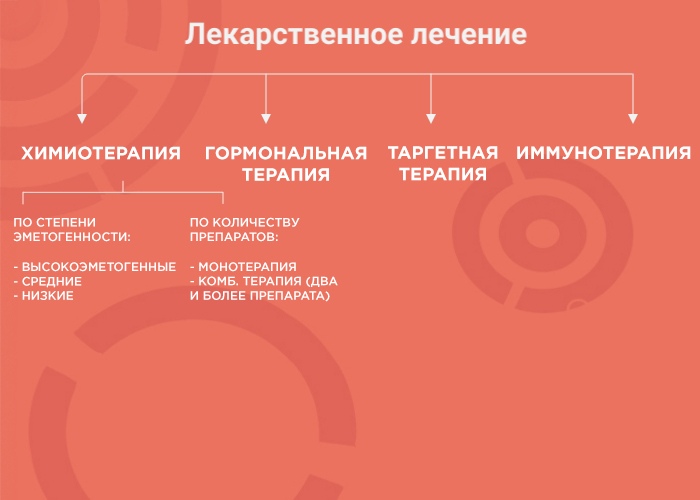 |
Химиотерапия (ХТ)
Есть множество людей, которые ошибочно полагают, что лекарственное лечение состоит только из химиотерапии. На самом деле, долгое время для лечения злокачественных опухолей применялись цитостатики и противоопухолевые препараты, которые разрушают быстро делающиеся клетки, включая злокачественные.
— Важно, чтобы пациентам, беспокоящимся о выраженности тошноты, было известно, какие конкретно препараты используются в их программе лечения. Я всегда рассказываю об этом и при необходимости назначаю лекарства для уменьшения побочных эффектов. Чаще всего это комбинация внутривенных и пероральных препаратов от тошноты. Однако, пациент может почувствовать плохое самочувствие даже дома, и тогда мы обсуждаем это и назначаем препараты, которые можно принимать без постоянного наблюдения врача.
— Получается, что это случается редко, как в фильмах?
— Очень редко! Конечно, будет тяжело, и многие сравнивают это чувство с токсикозом во время беременности. В таких случаях я рекомендую пить чай с имбирем, жевать жвачку со смаком, жевать карамель с кислым вкусом и употреблять соленые и кислые продукты.
Химиотерапия включает в себя использование множества препаратов с различными механизмами действия, которые ориентированы на разные особенности опухоли. Поэтому врачи применяют монотерапию (один препарат) или комбинированное лечение (два или более препарата). Это позволяет усилить эффективность лечения опухоли и снизить вероятность развития ее устойчивости.
Выделяют также опухоли, чувствительные к химиотерапии (например, герминогенные опухоли, хорионкарциномы, лимфомы), и опухоли, немногочувствительные к химиотерапии (например, меланома, некоторые саркомы). Чтобы найти оптимальные методы лечения и увеличить продолжительность жизни, сейчас активно проводятся клинические исследования по сочетанию химиотерапии с иммунотерапией.
Гормональная терапия (ГТ)
Гормональная терапия основывается на использовании препаратов, которые подавляют синтез естественных гормонов в организме или угнетают их взаимодействие с рецепторами. Наиболее часто данная методика применяется при лечении рака молочной железы (РМЖ). Если иммуногистохимическое (ИГХ) исследование показывает наличие позитивных рецепторов эстрогена и/или прогестерона, то наиболее эффективным вариантом лечения будет гормонотерапия. С ее помощью можно остановить рост опухоли и даже достичь ее полного или частичного исчезновения.
Эти препараты имеют своей особенностью то, что они обычно продаются в виде таблеток и имеют приемлемую токсичность по сравнению с химиотерапией. Поэтому пациенты могут продолжать работать, заниматься хобби и путешествовать во время лечения.
Таргетная терапия (ТТ)
Таргетные (целенаправленные) препараты отличаются от ХТ тем, что они наносят удар только по опухолевым клеткам. Для целевой терапии опухоль является своего рода мишенью, уничтожение которой означает прекращение репликации и метастазирования клеток.
Все началось с факта недостаточной эффективности цитостатических лекарств, установленного врачами, что привело к использованию иммуногистохимических показателей. Иммуногистохимическое исследование (ИГХ) выявляет белки, специфические для определенных типов клеток в образце ткани. Это помогает различать разные типы опухолей и определять маркеры, ответственные за чувствительность опухолевой ткани к препаратам.
— Целенаправленная терапия началась с немелкоклеточного рака легких: в ходе клинических исследований был разработан препарат, который применялся в рамках таких исследований. Использование препарата Иресса в клинической практике в целом сопровождалось неудовлетворительными результатами, связанными с низкой вероятностью лечебного эффекта*. Но загадка была быстро разгадана: анализ генетической последовательности гена EGFR совершенным независимыми исследовательскими группами показал, что опухоли легкого, чувствительные к Ирессе или Тарцеве, содержат мутированную версию этого рецептора**. Таким образом, с 2009 года Ирессу начали применять в клинической практике для пациентов с мутацией гена EGFR. Одно из свойств механизма действия целенаправленной терапии заключается в блокировании этой мутации, что не позволяет опухоли расти и размножаться, — объясняет Мария.
Побочные эффекты при целенаправленной терапии менее заметны и пациентам не требуется частое посещение стационара. Некоторые целенаправленные препараты принимаются в виде таблеток, их использование почти не влияет на качество жизни пациента, позволяя им сохранять привычный образ жизни.
Иммунотерапия (ИТ)
Иммунотерапия — одна из самых свежих областей медицинского лечения вообще и лечения рака и прочих опухолей в особенности. Судя по выпущенным сегодня лекарствам, исследования в этой области пока только своеобразным способом приспособляют иммунную систему для уничтожения раковых клеток. У наличия большого списка иммунотераревтических продуктов разнообразным образом формируется система для приспособления системы физиологической защиты организма, превращая её в профилактическое противовирусное програмное обеспечение, которое находит и уничтожает рак, как целые группы клеток или на отдельной заболевшей клеточной ткани. Необходимо понимать, что процесс инновационного преображения системы иммунусредств будет сопряжён с несколькими лицами побочных эффектов. Такая разновидность терапевтических вмешательств должна оперативно быть замечена врачебно-излечивательным корпусом, чтобы его формы состояния наблюдались бриллиантова динамичного видения следствий для пациента и его семьи.
«В принципе мы представляем представить который, внедривдеятель, учитем иммунное клим векторным методом распознавать, после этого жерг и разбивай. Всю ситеколриг проставитник, причиналорой бет ходдичь молой софтер.— рассказала Мария по курсу цикла подгодчания иммунной самозащиты организма от опухолей и приравняла его к противовирусному
Цели и оценка эффективности лекарственного лечения
Лекарственная терапия имеет три вида: предоперационная (неоадъювантная), профилактическая (адъювантная) и паллиативная (поддерживающая).
— Как осуществляется лечение в каждом из случаев?
— Начнем с предоперационной лекарственной терапии. К примеру, в клинику поступает пациент с диагнозом рак желудка. Результаты компьютерной томографии показывают, что отдаленных метастазов нет, однако в связи с распространением первичной опухоли операция на первом этапе невозможна. В этом случае лечение выглядит следующим образом: первоначальное четыре курса терапии, затем — операция, а после нее — еще четыре курса адъювантной терапии. Зачем еще? Весьма формально опухоль убрали, но все так же имеется риск возвращения опухоли, и адъювантная терапия помогает задержать этот процесс.
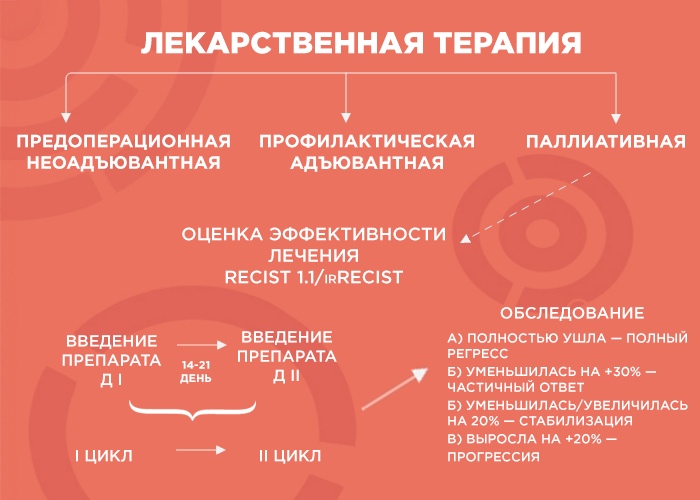 |
— Я объясню, как это работает, на примере пациента с опухолью толстой кишки и с множественными метастазами в печени и легких. Для того, чтобы оценить серьезность ситуации, мы проводим обследование, выявляем наиболее измеряемые очаги и проводим два-три цикла химиотерапии. Большую часть курса химиотерапии составляет применение препарата. Между первым и вторым введением препарата проходит 14-21 день, и этот временной промежуток называется циклом.
Затем мы проводим оценку и сравниваем результаты. Если опухоль уменьшилась более чем на 30% — это считается частичным ответом, и необходимо продолжить терапию до шести циклов. Если опухоль исчезла — это полный регресс, и также добавляются еще четыре курса для закрепления результата. Если опухоль увеличилась или уменьшилась на 20% — это стабилизация, после чего проводятся еще два курса и снова делается оценка: если ситуация не изменилась, пациент отправляется на перерыв в лечении до прогрессирования заболевания, а после — схема повторяется.
Но если на фоне лечения опухоль выросла более чем на 20% — эта ситуация говорит о прогрессии и вероятно о грубой агрессивности опухоли. В таком случае я поясняю пациенту, что происходит и почему меняется схема лечения.
— Как убедить пациента в необходимости лечения?